LISZI JÁNOS
A fizikai kémia történetéből
Második rész
Jedlik Ányos írta valamikor 1847 és 1851 között a következőket: “A meleg vagy alanyilag, vagy tárgyilag tekinthető. Alanyilag jelenti azon sajátságos érzetet, melyet testünknek bár melly részén veszünk észre, ha például befűtött kemenczéhez, vagy égő testhez közeledünk, vagy avval érintkezésbe jövünk. Tárgyilag vett meleg pedig nem egyéb, mint az imént említett érzetnek oka.” Itt az alanyilag vett meleg a hőérzet, a tárgyilag vett pedig maga a hő. Ma a termodinamikában a hő fogalmát szigorúan körülhatárolják: hőnek a kizárólag hőmérséklet-különbség hatására, munka nélkül a rendszer határán átmenő energiát értik. A hő és a munka egymásba átalakíthatók, amint azt a gőzgép példája is mutatja. A munka hőegyenértékét Rumford határozta meg elsőként.
Jedlik Ányos István (1800-1895)
Nagy magyar fizikus, bencés szerzetes. 1822-ben avatták a bölcsészet doktorává a Magyar Királyi Tudomány-Egyetemen. 1825-ben szentelték pappá. 53 évig tanított, ebből 37 és fél évig a pesti egyetemen. 1829-ben elkészítette a világ első elektromágneses motorját.
1830-ban ismertette a savanyú- és szódavíz gyártásának módját, sőt ő indította el a magyarországi szódavízipart. 1856-ban (Siemens előtt) rájött a dinamó elvére, 1859-ben már működött is készüléke. 21 éven keresztül foglalkozott optikai rácsokat előállító vonalzógép készítésével. Olyan gépet szerkesztett, amely 2093 vonalat volt képes milliméterenként előállítani. 1862 és 1865 között tükörpárból interferométert készített a fény hullámhosszának meghatározására. A készülék mintegy húsz évvel később újrafelfedezve Michelson-féle interferométerként vált világhírűvé. Számos európai egyetemen járt, találkozott többek között Clausiussal is. Sajnos, keveset publikált. Ehhez Poggendorf elutasító magatartása is hozzájárulhatott. Az történt, hogy 1863-ban nyolc leideni palackból olyan elektrosztatikus készüléket készített, amely 63 cm hosszúságú szikrát produkált. Ez akkoriban óriási eredmény volt. Barátai biztatására leírta a készüléket, és a kéziratot elküldte az Annalen der Physikhez publikálásra. Poggendorf, a folyóirat kiadója, levélben kioktatta, hogy találmánya nem új, ő maga is szerkesztett már hasonlót. 1878-ban visszavonult a pesti egyetemről, utódja báró Eötvös Loránd lett. 1895 végén hunyt el Győrben, sírjánál Eötvös Loránd mondott búcsúbeszédet.
Benjamin Thompson, később Rumford gróf (1753-1814)
Woburnban (Észak-Amerika) született és Auteuilben (Párizs mellett) halt meg. Eredetileg Thompsonnak hívták, a Rumford nevet akkor vette fel, amikor német birodalmi grófi rangra emelték. Részt vett az észak-amerikai szabadságharcban. Később Bajorországba került, ahol magas állami állásokban működött. Egy ideig a távol levő választófejedelem helyett vezette az ország ügyeit. Münchenben ágyúfúrással foglalkozott. Azt tapasztalta, hogy az egy ló által mozgatott fúró a fúrás során két és fél óra alatt annyi hőt fejlesztett, hogy az a jéghideg vizet felforralta. Megállapította, hogy a fúrás a fém semmilyen fizikai tulajdonságát nem változtatta meg. Ebből arra következtetett, hogy a hő nem lehet anyag, a mechanikai munka alakult át hővé. Méréseiből meghatározta a mechanikai munka hőegyenértékét.
Rudolf Julius Emmanuel Clausius (1822-1888)
Köslinben, Poroszországban született. A Berlini Egyetemen tanult. Halléban doktorált. 1855 és 1867 között a Zürichi Műegyetemen volt a matematikai fizika professzora. 1864-től haláláig a Bonni Egyetem tanára volt. Élete utolsó éveiben a Bonni Egyetem rektoraként működött. Termodinamikai munkáit alapvetően Zürichben végezte. Ő fedezte fel elsőként, hogy a redukált hő termodinamikai tulajdonság. Sőt az entrópia név is tőle származik (a görög εντροπη – irαnyt mutatni – kifejezésből ered.) Az elsők között ismerte fel a reverzibilis folyamatok fontosságát. Jelentős szerepe volt a második főtétel értelmezésében. (A termodinamika főtételeiről később lesz szó.) Így írt: “A hő sohasem megy hidegebb testből melegebb testbe.” “A világegyetem energiája állandó, entrópiája maximum felé tart.”
A termikus entrópia mint redukált hő
1. ábra. T-S diagram

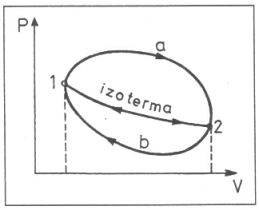 Ha egy folyamat kezdeti és végső állapota azonos, akkor körfolyamatról beszélünk. A 2. ábra két körfolyamatot mutat. Menjünk az a úton 1-ből 2-be. Az a görbe alatti terület a rendszer által végzett munkát mutatja. Ha 2-ből b úton visszamegyünk 1-be, akkor a folyamat bezárul, a b görbe alatti terület a rendszeren végzett munkát jelenti. A két görbe alatti terület különbsége a rendszerből kinyert munka. A 2. ábrán egy izotermát is berajzoltunk. Ha az izoterma mentén megyünk 1-ből 2-be, majd 2-ből 1-be, akkor izoterm körfolyamatról van szó. Ebben az esetben a rendszer által végzett munka nagysága azonos a rendszeren végzett munkáéval, de előjelük ellenkező. Az izoterm körfolyamat munkája tehát zérus. (Valójában itt izoterm reverzibilis folyamatról van szó. A reverzibilis (= megfordítható) folyamat minden határon túl kicsi nyomáskülönbségek hatására, minden határon túl lassan valósul meg. A termikus entrópiára vonatkozó egyenletben pedig a reverzibilis hőt kell szerepeltetnünk (∆S=qrev/T), ami minden határon túl kicsi hőmérséklet-különbségek hatására megy át a rendszer falán.)
Ha egy folyamat kezdeti és végső állapota azonos, akkor körfolyamatról beszélünk. A 2. ábra két körfolyamatot mutat. Menjünk az a úton 1-ből 2-be. Az a görbe alatti terület a rendszer által végzett munkát mutatja. Ha 2-ből b úton visszamegyünk 1-be, akkor a folyamat bezárul, a b görbe alatti terület a rendszeren végzett munkát jelenti. A két görbe alatti terület különbsége a rendszerből kinyert munka. A 2. ábrán egy izotermát is berajzoltunk. Ha az izoterma mentén megyünk 1-ből 2-be, majd 2-ből 1-be, akkor izoterm körfolyamatról van szó. Ebben az esetben a rendszer által végzett munka nagysága azonos a rendszeren végzett munkáéval, de előjelük ellenkező. Az izoterm körfolyamat munkája tehát zérus. (Valójában itt izoterm reverzibilis folyamatról van szó. A reverzibilis (= megfordítható) folyamat minden határon túl kicsi nyomáskülönbségek hatására, minden határon túl lassan valósul meg. A termikus entrópiára vonatkozó egyenletben pedig a reverzibilis hőt kell szerepeltetnünk (∆S=qrev/T), ami minden határon túl kicsi hőmérséklet-különbségek hatására megy át a rendszer falán.)
Temodinamikai hatásfok
3. ábra.A Carnot-körfolyamat
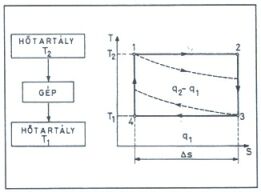 A hő és a munka egymásba átalakíthatók. Most azt vizsgáljuk, hogy mi az a legnagyobb hatásfok, amellyel a hő munkává alakítható. A tapasztalat azt mutatja, hogy hőből körfolyamatban lehet folyamatosan munkát nyerni. (Az előző rész 1. ábráján bemutatott dugattyú addig mozog, amíg a belső nyomás meg nem egyezik a külsővel, ekkor a folyamat megáll.) Láttuk, hogy az izoterm reverzibilis körfolyamat munkája zérus. Ezért a legnagyobb hatásfokú körfolyamatnak nem izotermnek (és reverzibilisnek) kell lennie. Ilyet szerkesztett Sadi Carnot. A Carnot-körfolyamathoz kell két hőtartály: egy meleg (T2) és egy hideg (T1), valamint egy rendszer (gép), ami a hőt munkává alakítja. Mindezt a megfelelő T–S diagrammal együtt mutatja a 3. ábra. A munkát adó rendszer egy teljes ciklus során a következő lépésekben működik.
A hő és a munka egymásba átalakíthatók. Most azt vizsgáljuk, hogy mi az a legnagyobb hatásfok, amellyel a hő munkává alakítható. A tapasztalat azt mutatja, hogy hőből körfolyamatban lehet folyamatosan munkát nyerni. (Az előző rész 1. ábráján bemutatott dugattyú addig mozog, amíg a belső nyomás meg nem egyezik a külsővel, ekkor a folyamat megáll.) Láttuk, hogy az izoterm reverzibilis körfolyamat munkája zérus. Ezért a legnagyobb hatásfokú körfolyamatnak nem izotermnek (és reverzibilisnek) kell lennie. Ilyet szerkesztett Sadi Carnot. A Carnot-körfolyamathoz kell két hőtartály: egy meleg (T2) és egy hideg (T1), valamint egy rendszer (gép), ami a hőt munkává alakítja. Mindezt a megfelelő T–S diagrammal együtt mutatja a 3. ábra. A munkát adó rendszer egy teljes ciklus során a következő lépésekben működik.
1. A gépet összekapcsoljuk a meleg hőtartállyal. A gép T2 hőmérsékleten q2 hőt vesz fel (az 1→2 egyenes alatti terület a T–S diagramban), és ennek megfelelő munkát végez.
2. A gépet elszigeteljük a hőtartályoktól. A gép további munkát végez, de most, mivel nincs hőforgalom, állandó az entrópia. A T–S diagram 2 pontjából eljutunk a 3 pontba.
3. A gépet összekapcsoljuk a hideg hőtartállyal. A gép
T1 hőmérsékleten lead q1 hőt és ennek megfelelő munkát végzünk a gépen (a 3→4 egyenes alatti terület a T–S diagramban ).4. A gépet elszigeteljük a hőtartályoktól. A gépen további munkát végzünk, de most nincs hőforgalom, ezért állandó az entrópia. A
4 pontból visszajutunk az 1 pontba. Ezzel bezárult a körfolyamat. A gép T2 hőmérsékleten fölvett q2 hőmennyiséget, T1 hőmérsékleten leadott q1 hőmennyiséget, munkavégzésre fordítódott q2–q1. Ezért a hatásfok: η=(q2–q1)/q2. Fölhasználva az entrópiaváltozás és a reverzibilis hő közötti kapcsolatot, valamint azt, hogy az 1→2 és a
3→4 részfolyamatok entrópiaváltozása abszolút értékben
megegyezik:
η=(T2∆S–T1∆S)/T2∆S=(T2–T1)/T2. A termodinamikai hatásfok tehát a hőmérséklethatároktól függ. Ha
T1→0, akkor η→1.
Az η=1 eset elvileg sem érhető el. Ha nem állandó T2 hőmérsékleten venné fel a rendszer a hőt, hanem közben csökkenne a hőmérséklet, akkor csökkenne a kinyerhető munka és a hatásfok is. Ugyancsak csökkenne η, ha a 3→4 lépésben (munkavégzés a rendszeren) növekedne a hőmérséklet. Ezeket az eseteket szaggatott vonalak mutatják az ábrán. Szintén csökkentené a hatásfokot, ha a 2→3 és a 4→1 lépésben nem lenne állandó az entrópia. A Carnot-körfolyamatnál nincs nagyobb hatásfokú körfolyamat. A valóságos gépek hatásfoka például súrlódási veszteségek miatt is kisebb.
Nicolas Leonard Sadi Carnot (1796-1832)
Párizsban született jeles család gyermekeként. Apja híres fizikus volt, egyik unokatestvére 1887-ben a harmadik Francia Köztársaság elnöke volt. Hadimérnökséget tanult az École Polytechnique-en. Néhány évi katonai szolgálat után Párizsba költözött, ahol termodinamikai kutatást folytatott. 1824-ben jelentette meg nevezetes könyvét, melynek címe: “Gondolatok a hő erejéről és a hő által működtetett gépekről. Ebben a könyvben írja le azt a híres termodinamikai körfolyamatot, amelyet ma Carnot-ciklusnak nevezünk. Érdekes, hogy a termodinamikai hatásfok közismert és korrekt egyenletét hamis premisszából kiindulva vezette le. Carnot úgy gondolta, hogy a hő – egy vízesés vizéhez hasonlóan – anyagként folyik a melegebb helyről a hidegebb helyre, miközben veszteség nélkül munkát szolgáltat. Rudolf Diesel a XIX. század végén, a később róla elnevezett motor tervezésekor a Carnot-féle termodinamikai hatásfok alapján dolgozott. Carnot egészsége mindig törékeny volt. 1832-ben 36 éves korábban kolerában meghalt. A kor szokásának megfelelően valamennyi személyes holmiját, közöttük kéziratait is, elégették. Sohasem fogjuk megtudni, mennyit tudott a hő természetéről és milyen közel jutott az entrópia fogalmához.
A klasszikus termodinamika összefüggéseit az első és a második főtételből vezetjük le. A főtételek a következő részben lépnek színre.
_________________________
Természet Világa 2006. február - Termodinamika